o2 electron configuration ,Electron Configuration for Oxygen (O) ,o2 electron configuration,In this article, we will discuss, O2, O2+, O2-, O22+, O22- Molecular orbital (MO) diagram and how to calculate their bond order Tingnan ang higit pa Enter Enchanted Garden, a beautifully crafted slot machine from RTG, who is a reputable developer of high-quality software for the online casinos. As it’s easy to guess from the title, this game will transport you to a fantastic .
0 · Molecular orbital diagram for O2
1 · Oxygen Electron Configuration and O2
2 · O 2
3 · What is the Electron Configuration of Oxygen Ion(O2
4 · Oxygen Orbital diagram, Electron configuration, and
5 · Electron Configuration for Oxygen (O)
6 · What is the electron configuration of the oxide ion O 2?
7 · Explain the formation of {O}
8 · What is the ground state electron configuration for
9 · How to Write the Electron Configuration for Oxygen?
Ang oxygen, na may simbolong O at atomic number 8, ay isang napakahalagang elemento sa ating mundo. Mula sa ating paghinga hanggang sa pagbuo ng tubig, ang oxygen ay gumaganap ng isang pangunahing papel. Ngunit, ang oxygen ay bihirang matagpuan sa kanyang atomic form. Karaniwan itong umiiral bilang diatomic molecule na O2, ang oxygen gas na kinakailangan para sa ating buhay. Upang maunawaan ang mga katangian at pag-uugali ng O2, mahalagang suriin ang kanyang electron configuration. Hindi lamang natin susuriin ang simpleng electron configuration ng oxygen atom, kundi pati na rin ang mas komplikadong molecular orbital configuration ng O2.
Bakit Mahalaga ang Electron Configuration?
Ang electron configuration ng isang atom o molecule ay naglalarawan sa pagkakaayos ng mga electron sa loob ng kanyang energetic levels at orbitals. Sa madaling salita, ito ang "address" ng bawat electron sa loob ng atom o molecule. Ang kaalamang ito ay kritikal dahil:
* Hinuhulaan nito ang Kemikal na Pag-uugali: Ang mga electron sa outer shell (valence electrons) ang responsable para sa kung paano nakikipag-ugnayan ang isang atom sa iba pang atom. Ang electron configuration ay tumutukoy sa bilang at uri ng mga valence electrons.
* Nagpapaliwanag ng Magnetic Properties: Ang pagkakaroon ng unpaired electrons ay nagdudulot ng paramagnetic properties, habang ang lahat ng paired electrons ay nagdudulot ng diamagnetic properties. Ang electron configuration ay nagpapakita kung mayroong unpaired electrons.
* Nakatutulong sa Pag-unawa ng Bonding: Ang paraan ng pagbabahagi o paglilipat ng electrons sa pagitan ng mga atom upang bumuo ng chemical bonds ay direktang nauugnay sa kanilang electron configuration.
* Nagpapaliwanag ng Spectral Properties: Ang paglipat ng electrons sa pagitan ng iba't ibang energy levels ay nagreresulta sa absorption o emission ng light. Ang electron configuration ay nagbibigay ng impormasyon tungkol sa mga energy levels na ito.
Electron Configuration ng Oxygen Atom (O)
Bago natin talakayin ang molecular orbital configuration ng O2, kailangan muna nating maintindihan ang electron configuration ng isang isolated oxygen atom (O).
Ang oxygen ay may 8 protons sa kanyang nucleus, na nangangahulugang mayroon din itong 8 electrons sa neutral state. Ang mga electrons na ito ay pumupuno sa energy levels at orbitals ayon sa Aufbau principle, Hund's rule, at Pauli exclusion principle.
* Aufbau Principle: Ang mga electrons ay pumupuno muna sa pinakamababang energy levels.
* Hund's Rule: Sa loob ng isang subshell (p, d, f), ang mga electrons ay pumupuno nang isa-isa sa bawat orbital bago magsimulang magpares. Ito ay upang i-maximize ang kabuuang spin.
* Pauli Exclusion Principle: Walang dalawang electrons sa isang atom ang maaaring magkaroon ng parehong set ng apat na quantum numbers. Ito ay nangangahulugang ang bawat orbital ay maaaring maglaman lamang ng maximum na dalawang electrons, na may magkasalungat na spins.
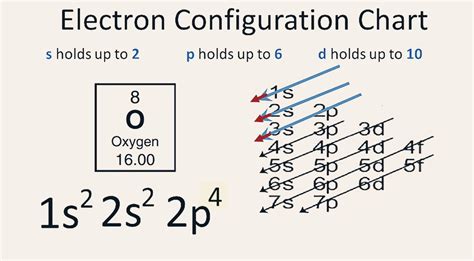
Gamit ang mga prinsipyong ito, ang electron configuration ng oxygen atom ay:
1s² 2s² 2p⁴
Ito ay nangangahulugang:
* 1s²: Dalawang electrons sa 1s orbital (ang pinakamababang energy level).
* 2s²: Dalawang electrons sa 2s orbital.
* 2p⁴: Apat na electrons sa 2p orbitals. Dahil mayroong tatlong 2p orbitals (2px, 2py, 2pz), ang Hund's rule ay nagsasaad na ang dalawa sa mga ito ay magkakaroon ng isang electron, at ang isa ay magkakaroon ng dalawang electrons. Kaya, mayroong dalawang unpaired electrons sa oxygen atom.
Electron Configuration ng Oxide Ion (O²⁻)
Ang oxide ion (O²⁻) ay nabubuo kapag ang oxygen atom ay nakakuha ng dalawang electrons. Ito ay upang makamit ang isang stable octet configuration (8 valence electrons), katulad ng noble gas na neon.
Ang electron configuration ng O²⁻ ay:
1s² 2s² 2p⁶
Sa configuration na ito, ang lahat ng orbitals ay fully filled, na nagreresulta sa isang stable at diamagnetic ion. Ang O²⁻ ay isoelectronic sa neon (Ne), na nangangahulugang mayroon silang parehong bilang ng electrons at parehong electron configuration.
Molecular Orbital Theory (MOT) at ang O2 Molecule
Ang pag-unawa sa electron configuration ng isolated oxygen atom ay mahalaga, ngunit upang lubos na maunawaan ang O2 molecule, kailangan nating gumamit ng Molecular Orbital Theory (MOT).
Ayon sa MOT, kapag ang dalawang atom ay nag-combine upang bumuo ng isang molecule, ang kanilang mga atomic orbitals ay nag-i-intersect at bumubuo ng mga bagong orbitals na tinatawag na molecular orbitals. Ang mga molecular orbitals na ito ay naka-spread sa buong molecule, hindi katulad ng atomic orbitals na naka-localize sa isang solong atom.
Ang MOT ay nagbibigay ng mas tumpak na paglalarawan ng bonding kaysa sa simple valence bond theory, lalo na para sa mga molecule na may resonance o delocalized electrons.
Molecular Orbital Diagram para sa O2
Para sa O2, ang atomic orbitals ng dalawang oxygen atoms ay nag-combine upang bumuo ng mga sumusunod na molecular orbitals:
* σ2s: Sigma 2s bonding molecular orbital (mas mababa sa energy kaysa sa atomic orbitals).
* σ*2s: Sigma 2s antibonding molecular orbital (mas mataas sa energy kaysa sa atomic orbitals).
* σ2p: Sigma 2p bonding molecular orbital.
* π2p: Pi 2p bonding molecular orbitals (dalawang degenerate orbitals).
* π*2p: Pi 2p antibonding molecular orbitals (dalawang degenerate orbitals).
 .jpg)
o2 electron configuration Slot Width Dual-slot Length 145 mm 215 mm 5.7 inches 8.5 inches TDP 75 W .
o2 electron configuration - Electron Configuration for Oxygen (O)